
研发团队合影。本版均为受访者供图
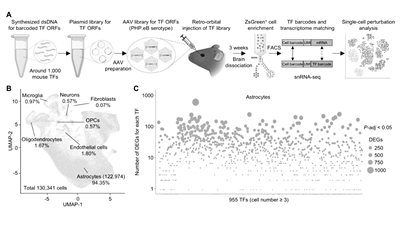
研究示意图。
在人类大脑中,除了神经元,还存在着数量庞大的星形胶质细胞。它们像“守护星”一样,支持着神经元的正常运作。然而在阿尔茨海默病等神经退行性疾病中,这些“守护者”也会“黑化”,释放毒素加速神经元的死亡。
能否将这些“失控的守护星”重新“驯化”,让它们恢复保护功能?关键在于找到控制其命运与行为的核心“开关”——转录因子。这类分子如同细胞内的“总指挥”,能够调控成千上万基因的表达。然而,人类基因组中转录因子超过1000种,究竟哪些才能真正决定星形胶质细胞的状态,长期以来难以系统分析,科学家只能一个个排查,效率极低。如今,这一难题被上海科学家攻克。青年报记者 刘晶晶
从上千个目标中锁定关键因子
4月24日凌晨,中国科学院脑科学与智能技术卓越创新中心周海波研究团队,联合上海市第六人民医院郑元义教授团队与上海鲸奇生物胡新德研究团队,在国际顶级期刊《科学》(Science)发表最新研究成果。
团队开发出一种名为iGOF-Perturb-seq的体内高通量功能获得性扰动测序平台,首次系统性绘制了小鼠大脑星形胶质细胞的转录因子功能图谱,并从中筛选出可有效改善阿尔茨海默病认知损伤的“刹车”基因——转录因子 Ferd3l。
研究团队通过携带星形胶质细胞特异性启动子的腺相关病毒(AAV)载体,让其像“智能快递员”一样,将近1000个转录因子的“指令包”分别精确送入小鼠的星形胶质细胞中,每个“指令包”都自带一个独特的“条形码”身份证。
随后,科学家用单细胞测序技术,读取了近40万个星形胶质细胞的转录组“工作日志”,并通过条形码将每个细胞的状态与它收到的指令一一对应。
“我们建立了一套在体内高通量研究基因功能获得性效应的新技术。”论文通讯作者周海波研究员介绍,“通过这套技术,我们研究了大约1000种转录因子在星形胶质细胞中的功能,从而绘制出了星形胶质细胞转录因子的系统性功能图谱。”
这张图谱不仅呈现了转录因子与靶基因的调控关系,更识别出多个具有协同调控作用的功能模块,并为此前功能未知的转录因子进行了功能注释。这相当于一张巨大的“藏宝图”,帮助科学家快速筛选出能抑制星形胶质细胞“黑化”的候选因子。
“实战筛选”关键靶点
与以往研究不同,该团队首次在模拟疾病的病理条件下进行了第二轮筛选。
“利用数据库与多种神经退行性疾病、正常衰老及精神疾病患者的数据进行关联分析后,我们预测了一批疾病相关的候选转录因子。”周海波解释,“但这些因子在疾病状态下能否真正阻止星形胶质细胞恶化,在正常条件下筛选是做不到的。”
研究团队利用一个模拟神经炎症的小鼠模型,对预测的疾病相关转录因子进行“实战测试”。结果,他们发现了一个最出色的“保护师”——转录因子Ferd3l。
在模拟人类阿尔茨海默病的小鼠模型中,通过静脉注射让Ferd3l“指令包”在全脑星形胶质细胞中起效后,这些小鼠的认知能力显著改善,在新物体识别和Y迷宫测试中接近健康小鼠。
深入分析发现,Ferd3l不仅让星形胶质细胞本身变得“温和”,还重建了它们与神经元、小胶质细胞等其他脑细胞之间的健康对话,让原本混乱、充满攻击性的脑内环境恢复成有序协作网络。
多学科交叉联合技术攻关
这一成果背后,是长达数年的技术积累与跨团队协作。
“体外实验相对简单,我们可以让每个细胞均匀感染一个因子。但到了体内就特别难了。”周海波坦言。如何将扰动基因通过病毒载体注射到血液中,并以合适的感染条件进入大脑细胞?如何精准地分离出被感染的细胞?如何读取每个细胞携带的条形码信息?每一项都是极为复杂的技术挑战。
然而,体外体系往往不能模拟真实的生理和病理状态,这正是必须攻克体内技术的根本原因。“我们为什么一定要做体内?因为体内有各种各样的接近真实环境的模型,呈现更接近真实的情况。”周海波说。
这项工作的数据规模庞大,仅附图就超过30张。论文第一作者张连升博士在项目统筹与技术整合中发挥了关键作用。
这是一个高度交叉的系统工程,需要不同专长的成员密切协作,周海波表示,团队成员分别在实验操作、数据分析、体内操作等方面各有所长,不同背景的科研人员紧密协作,加上合作单位在AAV病毒载体上的支持,才得以高效协同推进这项庞大工程。
“靶点库”拓展未来研究范围
与现有主要针对β淀粉样蛋白沉积的药物不同,该研究聚焦于星形胶质细胞这一层次。“阿尔茨海默病有多层次问题,未来联合使用不同层次的药物有可能实现更强的治疗效果。”周海波说。
这项研究,不仅为阿尔茨海默病找到了一颗“希望之星”,更重要的是,它开创了一条从体内高通量筛选到疾病模型验证的完整路径,为攻克多种难治性脑疾病提供了全新的武器库。
需要注意的是,目前该疗法仅在小鼠疾病模型中获得初步验证,距离临床应用仍有很大距离。其能否进一步发展为安全有效的治疗手段,尚需系统评估。例如,能否在大动物模型中得到验证、其长期安全性如何,以及相关靶点能否实现对人脑的有效递送等关键问题,仍有待进一步研究。
不过,这项研究的意义并不局限于单一疾病。
目前,大部分神经系统疾病都没有非常好的治疗药物。“创新药研发最大的‘卡脖子’点就是没有好的靶点。”周海波表示,“我们这项研究恰恰提供了一个靶点库,有1000个潜在靶点可以供大家选择。利用这套技术,未来还可以扩展库的范围,为更多疾病预测干预靶点。”
此外,研究团队计划将数据公开,全世界从事神经系统疾病研究的科学家或药企,都可以利用这个数据库寻找自己关注的靶点。
未来,该项技术还有望应用至帕金森病、渐冻症甚至抑郁症等疾病的研究与治疗。“我们实验室对帕金森病也非常感兴趣。”周海波说,“我们会尝试扩展库的应用,研究重度抑郁症等与星形胶质细胞极为相关的疾病治疗。”
